本文結(jié)合變更已上市藥品有效期補充申請的技術(shù)審評情況,對已上市藥品變更有效期審評要點進行歸納總結(jié),供研究者進行變更有效期撰寫申報資料參考,以期更好設(shè)計試驗,控制藥品質(zhì)量,提高申報效率。...
發(fā)布時間:2021-06-28
6 月 22 日,CDE 官網(wǎng)發(fā)布 2020 年藥審報告, 全年有 59 件新冠病毒疫苗和新冠肺炎治療藥物的注冊申請被納入特別審批程序并完成技術(shù)審評;受理 1 類創(chuàng)新藥注冊申請共 1062 件(597 個品種),審評通過新藥上市申請 208...
發(fā)布時間:2021-06-28
2019年10月24日,國家醫(yī)療保障局正式發(fā)布《關(guān)于印發(fā)疾病診斷相關(guān)分組(DRG)付費國家試點技術(shù)規(guī)范和分組方案的通知》(醫(yī)保辦發(fā)﹝2019﹞36號),同時發(fā)布《國家醫(yī)療保障DRG分組與付費技術(shù)規(guī)范》《國家醫(yī)療保障DRG(CHS-DRG)分...
發(fā)布時間:2019-12-20
自2019年12月1日起,在廣東省藥品上市許可持有人試點工作期間獲準成為藥品上市許可持有人的,其權(quán)屬不變;其它持有藥品批準文號的生產(chǎn)企業(yè)直接成為藥品上市許可持有人。
2019年12月1日前受理的GMP、GSP認證申請,按照原藥品G...
發(fā)布時間:2019-12-20
醫(yī)藥網(wǎng)2月20日訊 國務(wù)院新聞辦公室于2月19日(星期二)下午3時舉行國務(wù)院政策例行吹風(fēng)會,請國家衛(wèi)生健康委員會副主任李斌和財政部、國家醫(yī)療保障局、國家藥品監(jiān)督管理局有關(guān)負責(zé)人介紹癌癥防治工作和藥品稅收優(yōu)惠政策有關(guān)情況,并答記者問。國家衛(wèi)...
發(fā)布時間:2019-02-20
來源于國家食品藥品監(jiān)督管理總局食品藥品審核查驗中心
...
發(fā)布時間:2018-07-20
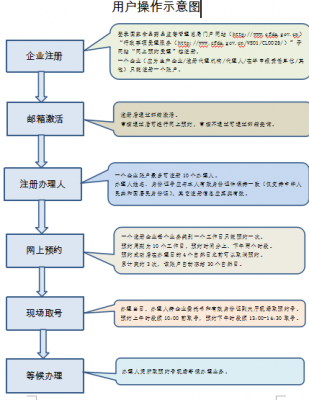
為了深化“放管服”改革,加快“互聯(lián)網(wǎng)+政務(wù)服務(wù)”工作步伐,推動食品藥品行政受理改革提質(zhì)增效,為行政相對人提供更加高效便捷的服務(wù),國家食品藥品監(jiān)督管理總局行政受理服務(wù)大廳(下稱大廳)網(wǎng)上預(yù)約受理系統(tǒng)將于近期上線運行。...
發(fā)布時間:2018-07-20
為進一步落實中共中央辦公廳、國務(wù)院辦公廳《關(guān)于深化審評審批制度改革鼓勵藥品醫(yī)療器械創(chuàng)新的意見》(廳字〔2017〕42號),簡化、優(yōu)化醫(yī)療器械延續(xù)注冊、臨床試驗審批,提高審評審批效率,國家藥品監(jiān)督管理局組織對醫(yī)療器械延續(xù)注冊等部分申報資料要求...
發(fā)布時間:2018-05-23
為落實中共中央辦公廳、國務(wù)院辦公廳《關(guān)于深化審評審批制度改革鼓勵藥品醫(yī)療器械創(chuàng)新的意見》(廳字〔2017〕42號)的要求,嚴格藥品注射劑審評審批,保障藥品安全、有效,國家藥品監(jiān)督管理局決定加強對化學(xué)仿制藥注射劑注冊申請開展現(xiàn)場檢查。有關(guān)事宜...
發(fā)布時間:2018-05-23